Milline kujutluspilt teile seoses kanepi tarvitamisega esimesena pähe tuleb? On see filmidest tuttav lõbus ajaveetmine sõprade seltsis või kodus lõõgastumine pärast pingelist tööpäeva? Paljude jaoks on siiski reaalsus teine, sest regulaarsel kanepi tarvitamisel on oma tume pool.
Kanep on maailmas üks enim tarvitatud illegaalseid aineid ja umbes 10% kanepi tarvitajatest teeb seda iga päev. 2024. aastal Ameerika Ühendriikides tehtud uuring näitas, et igapäevane kanepitarvitamine on levinum kui igapäevane alkoholi pruukimine.
Kanepitaimes on tuvastatud üle saja kannabinoidi, millest peamine on psühhoaktiivse toimega delta-tetrahüdrokannabinool (THC). Muu hulgas vahendab THC kanepi heaolu- ja mõnutundega seotud efekte ja sellel on oluline osa sõltuvuse tekkes.
Kümneid kordi kangem
Muret tekitab see, et viimase 50 aasta jooksul on THC sisaldus tarvitatavas kanepis aretusmeetodite ja kasvatustehnika muutumise tõttu suurenenud. Kui 1970-ndatel oli selle keskmine sisaldus umbes 1%, siis nüüd võib turult leida tooteid, kus see on koguni 20–30%.
Selle sajandi algul tehtud uuringuid, kus leiti, et kroonilisel kanepitarvitamisel ei ole pikaajalisi neuroloogilisi ega psühhiaatrilisi kõrvaltoimeid, ei pea kõrvale heitma. Tänapäevase kanepi mõju organismile ei saa aga varasemate aastakümnete omaga võrrelda. Seega on meil juurde vaja uuringuid just suure THC sisaldusega kanepi pikaajalise tarvitamise võimaliku mõju kohta.
Viimase aja teadusuuringutes on näidatud, et THC suure sisaldusega kanepi tarvitamine on nii sõltuvushäire kui ka psühhiaatriliste häirete nagu skisofreenia ja psühhooside riskitegur. Sõltuvushäire kujuneb välja paljude organismis toimuvate muutuste tulemusena, mida mõjutab sõltuvust tekitava aine korduv kasutamine. Kui kanepist nüüd sõltuvusse jäädakse, ei suudeta enam ilma selleta hakkama saada.

Minu teadustöö keskendub epigeneetilisele lähenemisele – sellele, kuidas eri tegurid, sh keskkonnategurid, mõjutavad geenide avaldumist. Epigeneetilise regulatsiooni tulemusena ei muutu DNA nukleotiidne järjestus, kuid need muutused võivad oluliselt mõjutada seda, millised geenid on n-ö aktiivsed või vaigistatud.
Soovin teada saada, kas korduv kokkupuude THC suurema kontsentratsiooniga põhjustab geenide avaldumises muutusi, mida väiksema kontsentratsiooniga ei teki. Täpsemalt keskendun ühele epigeneetilisele mehhanismile nimega DNA metülatsioon ja demetülatsioon, mille käigus geenide avaldumist mõjutatakse DNA-le metüülrühmade lisamise või nende eemaldamise kaudu. DNA metülatsiooni viivad läbi ensüümid, mida kutsutakse DNA metüültransferaasideks (DNMT-d), ja aktiivset DNA demetülatsiooni vahendavad TET metüültsütosiini dioksügenaasi perekonna ensüümid (TET – ingl ten-eleven translocation).
Geeniraamatul keeld peal
Me võime seda kirjeldada näiteks kui raamatukogu, kus üks raamat tähistab üht geeni. DNA metülatsiooni käigus pannakse osale raamatutele silt „Mitte lugeda“ ja selles raamatus olev teave jäetakse kõrvale – geen vaigistatakse. DNA demetülatsioon on mitmeetapiline protsess, mille käigus võetakse need sildid ära. See võimaldab raamatut taas lugeda, s.t geen muutub jälle aktiivseks.
Selleks et teha kindlaks, kuidas THC suurem kontsentratsioon geenide avaldumist mõjutab, tegin katseid tervete täisealiste vabatahtlike doonorite vererakkudega, mida sain Tartu Ülikooli Kliinikumi verekeskuse kaudu. Niisiis ei olnud tegemist kanepi tarvitajate vererakkudega, vaid modelleerisin kanepi tarvitamist katseklaasis.
Töötlesin rakke korduvalt nii väiksema kui ka suurema kontsentratsiooniga THC-ga, kasutades kaht katseskeemi: esiteks korduvad THC töötlused ning teiseks korduvad THC töötlused, millele järgneb töötlusevaba periood ja seejärel veel üks THC töötlus. Eesmärk oli leida vastus küsimusele, kas THC suurem kontsentratsioon põhjustab DNA metülatsioonis ja demetülatsioonis muutusi, mida väiksem kontsentratsioon ei põhjusta.
Mõned geenid võivad pärast korduvat kokkupuudet suures kontsentratsioonis THC-ga olla aktiivsemad kui tavaolukorras. Tekkivad kõrvalekalded võivadki soosida sõltuvushäire väljakujunemist.
Tulemused kinnitasid, et häired mehhanismides, mis mõjutavad geenide avaldumist, sõltuvad THC kontsentratsioonist inimese vererakkudes. Pärast korduvaid suure kontsentratsiooniga töötlusi nägime uurimisrühmaga DNA metülatsioonis ja demetülatsioonis muutusi, mida väiksema kontsentratsiooni korral polnud. Vererakkudes suurenes TET ensüümide aktiivsus ehk sagenes siltide „Mitte lugeda“ eemaldamine raamatutelt. Selle tulemusena kasvas pärast korduvaid töötlusi ülegenoomselt hüdroksümetülatsiooni osakaal, mis tähendab aktiivses demetülatsiooniprotsessis esimest etappi. Teisisõnu oli pärast korduvaid THC töötlusi selles rühmas rohkem geene aktiveerumisprotsessi – raamatutelt siltide eemaldamise – esimeses etapis.
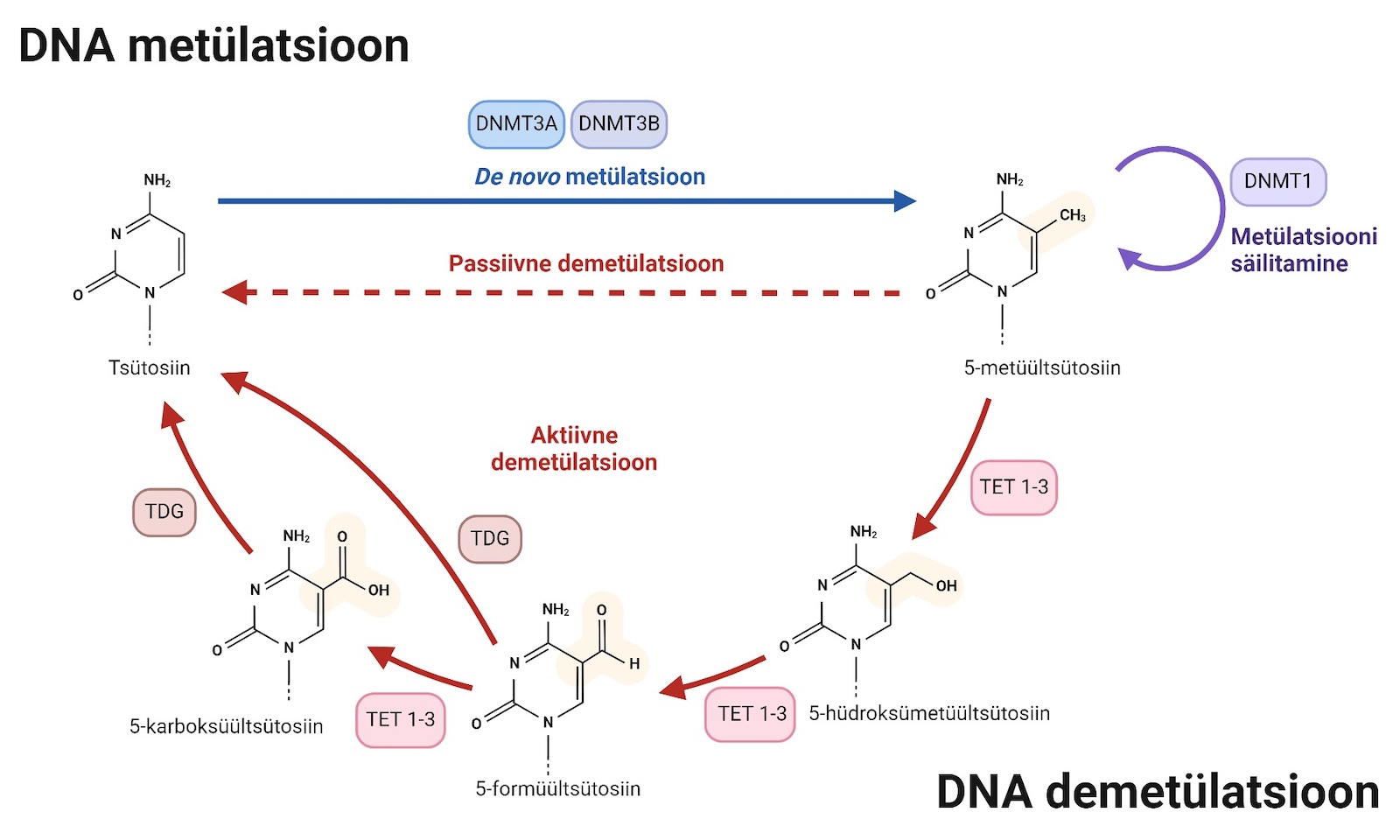
Pärast THC lisatöötlust aga vähenes vererakkudes ülegenoomselt hüdroksümetülatsiooni osakaal, mis näitab vahepealsel pausiperioodil demetülatsiooniprotsessi edasiliikumist järgmistesse etappidesse. S.t pärast THC lisatöötlust oli suurem osa geene esimesest etapist edasi liikunud, mis viibki lõpuks metüülmärgise eemaldamiseni ja nende geenide aktiveerumiseni.
Niisiis võivad mõned geenid pärast korduvat kokkupuudet suures kontsentratsioonis THC-ga olla aktiivsemad kui tavaolukorras. Tekkivad kõrvalekalded geenide regulatsioonis võivadki soosida sõltuvushäire väljakujunemist.
Varem on epigeneetiliste mehhanismide muutusi uuritud pärast korduvat kokkupuudet psühhostimulaatoritega nagu amfetamiin ja kokaiin. THC suure sisaldusega kanep on seni tähelepanu alt kõrvale jäänud, kuigi selle tarbimine on märgatavalt kasvanud.
Praegu pole veel piisavalt uuringuid, et teha lõplikke järeldusi THC suure sisaldusega kanepi pikaajalise ohtlikkuse või ohutuse kohta. Muutused geenide regulatsioonis võivad pikas plaanis mõjutada seda, miks mõni inimene jääb kanepist sõltuvusse ja teine mitte.
Uuring on avaldatud ajakirjas Translational Psychiatry.










